STRATIFICATION DU RISQUE ET PRONOSTIC
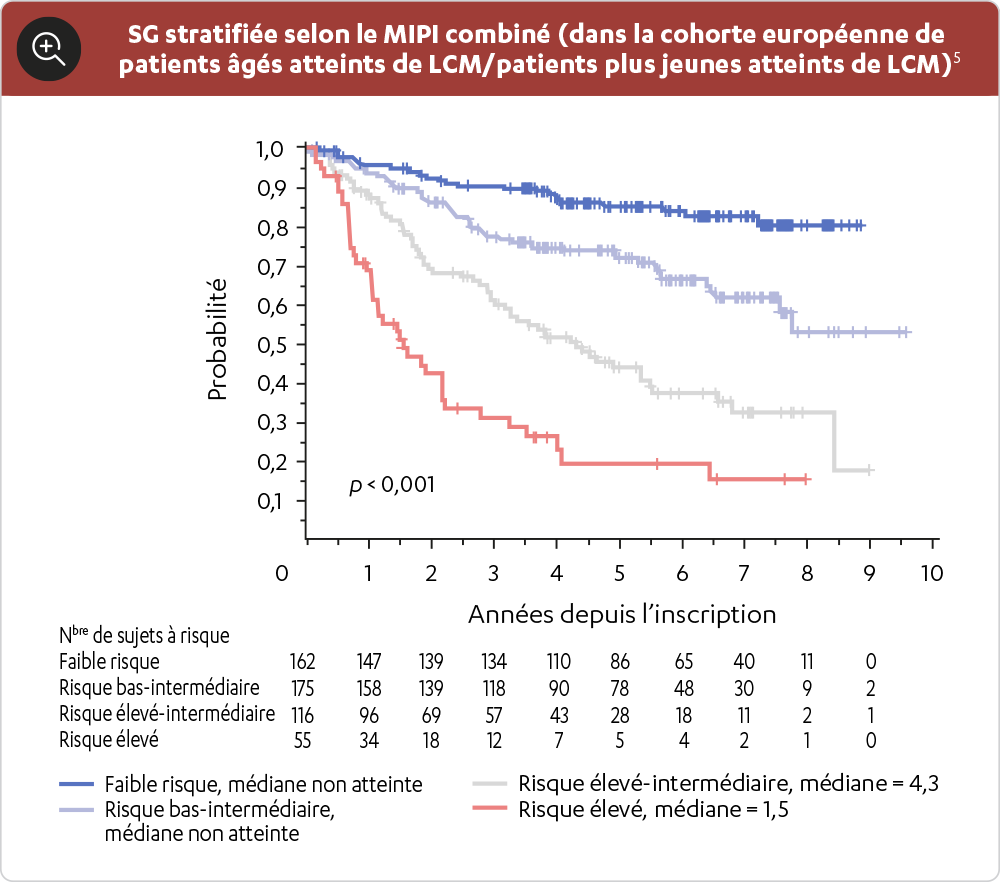
Comme le traitement pourrait différer selon le stade de la maladie, une évaluation approfondie doit être réalisée lors de la stadification initiale1,2. Le score MIPI est basé sur plusieurs facteurs pronostiques indépendants au moment du diagnostic, y compris les suivants : âge, indice fonctionnel ECOG, taux de LDH et numération leucocytaire. Dans une étude, un score MIPI de risque élevé était associé à une survie inférieure1,2.
À des fins de traitement, le LCM a été classé en deux sous-groupes principaux; ces sous-groupes sont désormais inclus dans la classification 2016 révisée de l’OMS concernant les affections lymphoïdes malignes3.
Les sous-groupes de LCM sont distincts dans le tableau clinique et les caractéristiques moléculaires3.
-
LCM classique3
- Il s’agit d’une variante extra-ganglionnaire/ganglionnaire volumineuse avec une évolution agressive de la maladie.
-
LCM non ganglionnaire leucémique et extra-ganglionnaire/ganglionnaire latent3
- On l’observe chez 10 à 20 % des patients atteints de LCM.
- Dans la plupart des cas, il est généralement associé à une évolution indolente de la maladie et à des résultats supérieurs.
- On l’observe chez 10 à 20 % des patients atteints de LCM.
STRATIFICATION DU RISQUE SELON LE MIPI
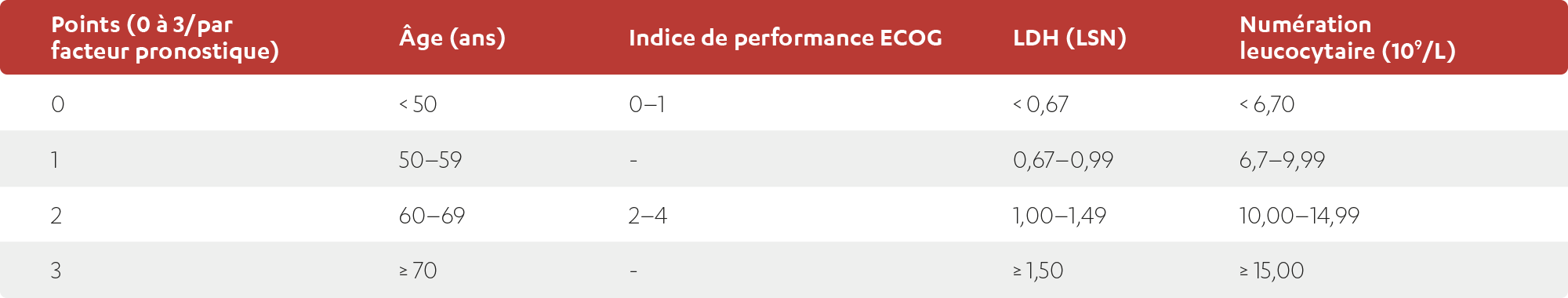
| Points (0 à 3/par facteur pronostique) | Âge (ans) | Indice de fonctionnel | LDH (LSN) | Numération leucocytaire (109/L) |
|---|---|---|---|---|
| 0 | < 50 | 0–1 | < 0,67 | < 6,70 |
| 1 | 50–59 | 0,67–0,99 | 6,7–9,99 | |
| 2 | 60–69 | 2–4 | 1,00–1,49 | 10,00–14,99 |
| 3 | ≥ 70 | ≥ 1,50 | ≥ 15,00 |
D’après la Société de leucémie et lymphome.
ECOG = Eastern Cooperative Oncology Group; LDH = lactate déshydrogénase; LSN = limite supérieure de la normale.
Pour chaque facteur pronostique, 0 à 3 points ont été attribués à chaque patient pour un nombre maximal de 11 points2.
- Les patients ayant 0 à 3 points au total étaient classés comme à faible risque, ceux ayant 4 ou 5 points, à risque intermédiaire, et ceux ayant 6 à 11 points, à risque élevé2.
- L’indice de fonctionnel ECOG a été pondéré de 2 points si les patients étaient alités ou incapables de travailler (ECOG de 2 à 4)4.
- Le taux de LDH a été pondéré selon le rapport de la LSN4.
- Par exemple, pour une LSN de 240 U/L, les limites étaient de 180, 240 et 360 U/L pour les groupes à faible risque, à risque intermédiaire et à risque élevé, respectivement.
Cette évaluation du risque peut aider à planifier les prochaines étapes de traitement du LCM en la divisant en1,3 :
- Maladie indolente – observation vigilante
ou
- Maladie agressive – traitement actif
ou
- Maladie récidivante/réfractaire – traitement actif
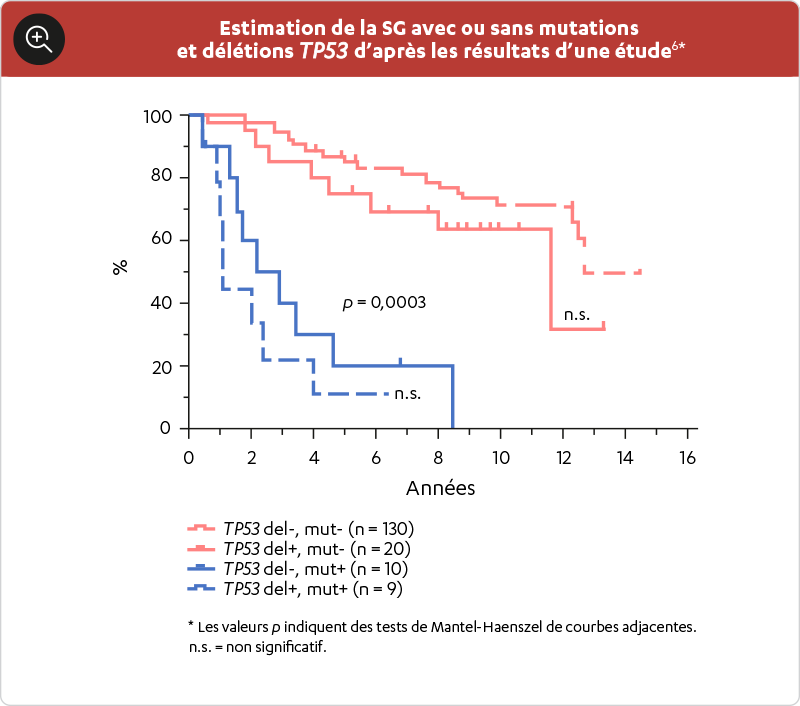
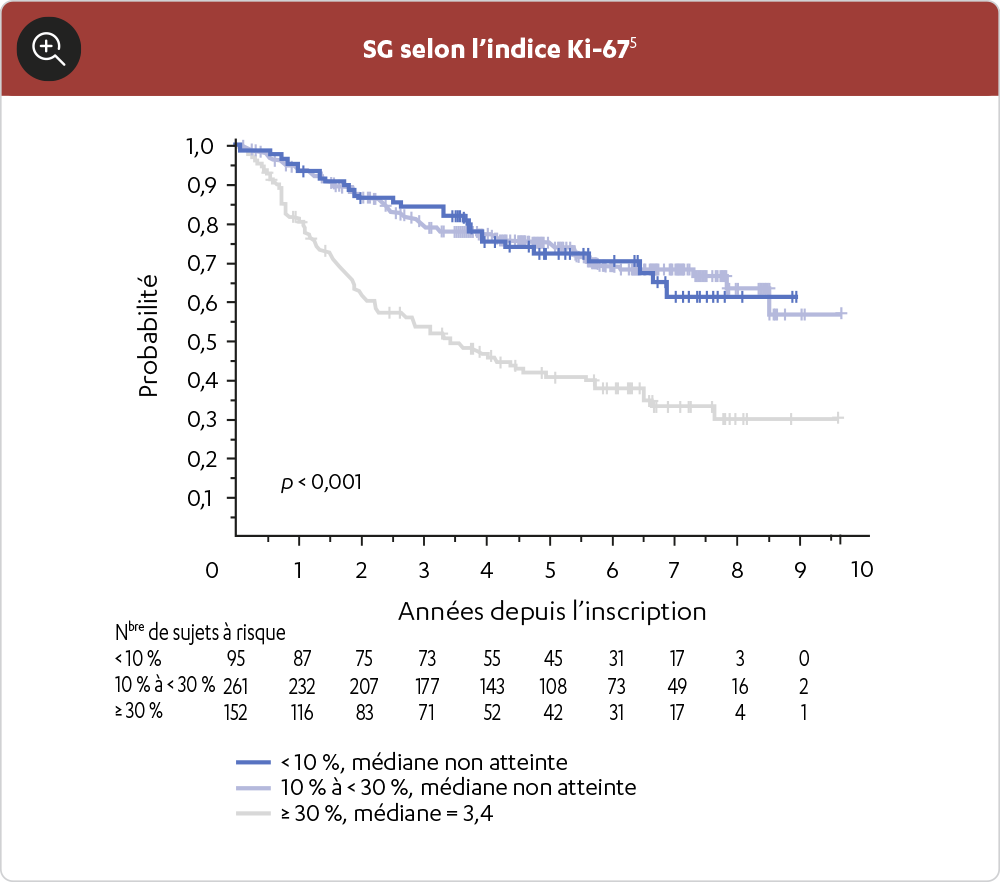
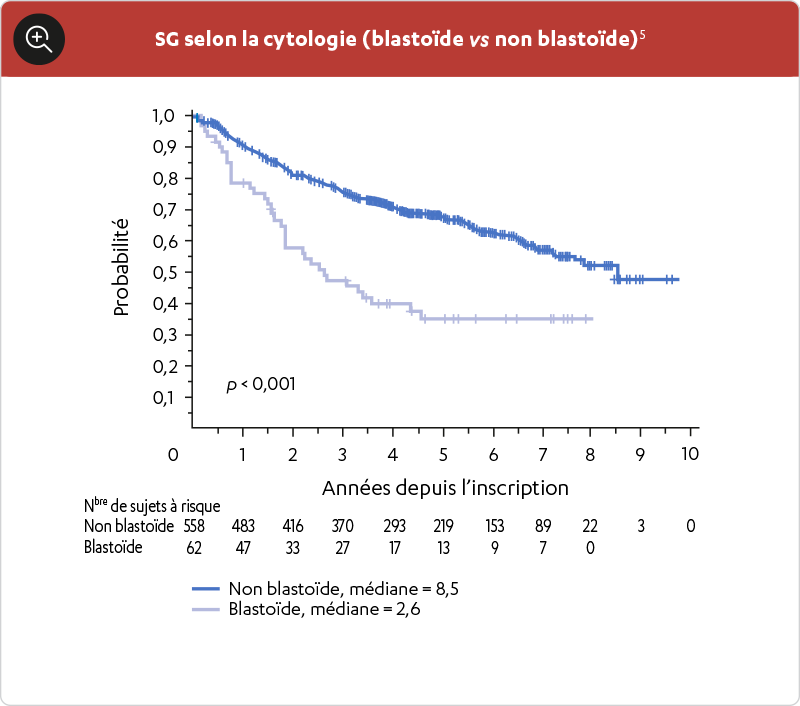
ON A MONTRÉ QUE CERTAINES CARACTÉRISTIQUES CLINIQUES ET MOLÉCULAIRES, COMME UNE MORPHOLOGIE BLASTOÏDE, UN SCORE MIPI DE RISQUE ÉLEVÉ ET UN INDICE KI-67 ÉLEVÉ, AIDENT À PRÉDIRE LES RÉSULTATS DES PATIENTS ATTEINTS DE LCM1
LE PROCESSUS DIAGNOSTIQUE LIÉ AU LCM
Les indices de stadification et de pronostic, comme le MIPI, peuvent aider à déterminer les stratégies thérapeutiques appropriées en fonction des facteurs de risque propres à chaque patient2.
Étant donné la nature agressive du LCM, environ 70 à 80 % des patients sont symptomatiques et nécessitent un traitement immédiatement à la suite du diagnostic et de la stadification (tableau 3)2,3.

| Patients présentant une maladie asymptomatique/indolente 1–3 | Patients présentant une maladie symptomatique/agressive 1,2 |
|---|---|
Ils peuvent faire l’objet d’une surveillance initiale en toute sécurité sans aucun compromis sur les
résultats à long terme.
|
Le choix du traitement est basé sur l’âge et la forme physique du patient.
|
RÉFÉRENCES :
- Cité en référence avec l’autorisation de NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®) for B-Cell Lymphomas V.1.2022 – 2 mars 2022. © National Comprehensive Cancer Network, Inc. 2022. Tous droits réservés. Consulté le 4 mars 2022. Pour consulter la plus récente version complète des recommandations du NCCN, visitez le site NCCN.org. Le NCCN n’offre aucune garantie quant à leur contenu, leur utilisation ou leur application, et décline toute responsabilité relative à leur application ou leur utilisation de quelque façon que ce soit.
- Société de leucémie et lymphome. Lymphome à cellules du manteau. En ligne à l’adresse : https://www.lls.org/sites/default/files/National/USA/Pdf/Publications/FS4F_FR_MCL_Facts_2018.pdf. Consulté le 24 août 2021.
- Jain P, Wang M. Mantle cell lymphoma: 2019 update on the diagnosis, pathogenesis, prognostication, and management. Am J Hematol 2019;94:710–25. Am J Hematol 2019;94:710–25.
- Hoster E, et al. A new prognostic index (MIPI) for patients with advanced-stage mantle cell lymphoma. Blood 2008;111(2):558–65.
- Hoster E, et al. Prognostic Value of Ki-67 Index, Cytology, and Growth Pattern in Mantle-Cell Lymphoma: Results From Randomized Trials of the European Mantle Cell Lymphoma Network. J Clin Oncol 2016; 34:1386–94. .
- Eskelund CW. TP53 mutations identify younger mantle cell lymphoma patients who do not benefit from intensive chemoimmunotherapy. Blood 2017;130(1):1903–10.